プレスリリース
国立研究開発法人海洋研究開発機構
Human Frontier Science Program
超簡単に短時間で人工細胞を作製する手法を確立
―人工細胞実験試薬のキット化に向けて―
1. 発表のポイント
- ◆
- 生きた細胞を模倣した人工細胞の作製に重要な脂質膜カプセルを、特別な装置の使用なしに30分以内に再現性よく形成する手法を確立した。
- ◆
- 人工細胞を作製するために必要な試薬を乾燥することで保存や輸送が簡便になり、また研究室外での実験も可能になった。
- ◆
- 本研究により、従来の方法よりも簡単かつ迅速に人工細胞を構築する手法が確立されたことで、誰でも簡単に人工細胞実験ができるキット化の目処がたった。
- ◆
- 例えば、特定のウイルスや生物のDNAがサンプル中に存在するかどうかを判別するバイオセンサーとしての応用などが将来的に期待できる。
2. 概要
国立研究開発法人海洋研究開発機構(理事長 大和 裕幸、以下「JAMSTEC」という。)超先鋭研究開発部門の車兪澈 副主任研究員らは、これまでよりも短時間で再現性よく人工細胞を作製する手法を確立しました。
タンパク質やDNAなどを組み合わせて擬似細胞を組み立てる人工細胞研究は、無生物から生物が創られるその仕組みを理解する研究として注目されています。また、応用面でも次世代のバイオエンジニアリングとして期待されている技術です。人工細胞は、脂質と呼ばれる分子がカプセル状の人工細胞膜を形成し、この内部にさまざまな分子を閉じ込めて、タンパク質合成などの生化学的な反応を行います(図1、2)。しかし、再現性よく質の高い膜を形成することは難しく、また、膜の形成には数時間から1日以上を要することから、時間の短縮も課題でした。
人工細胞膜の形成には脂質を均質に溶かしたオイルを用意することが重要ですが、本研究グループは「ガラス管の中で簡易的に脂質フィルムを作り、オイルを加えたあと70度で1分間温めてすぐに撹拌するという方法(図3)」へと従来の方法から単純化することで、形成時間を大幅に短縮することに成功しました。また、人工細胞膜に内包するタンパク質合成のための反応液をあらかじめ凍結乾燥することでより早く人工細胞を形成することが可能となり、これらの技術により30分以内で再現性よく、DNAからタンパク質を合成する人工細胞を作製できるようになりました。
脂質フィルムと乾燥試薬は常温で運搬することが可能であり、研究室外での実験が容易になることから、病原菌やウイルスの検査キットとしての応用も将来的に期待されます。また、必要な試薬をキット化することで、研究の場だけでなく学校などの理科学教育の場でも広く利用することができます。
本成果は、「Frontiers in Bioengineering and Biotechnology」に4月7日付け(日本時間)で掲載される予定です。なお、本研究はJST戦略的創造研究推進事業さきがけ(JPMJPR18K5)、JSPS科研費(16H06156、16KK0161、16H00797、21H05156)およびHuman Frontier Science Program(RGP0029/2020)のサポートを受けて実施されました。
- 国立研究開発法人海洋研究開発機構
- 東洋大学
- JSTさきがけ
- 横浜市立大学
特願2022-033672 膜脂質小胞の製造方法
3. 背景
生物は例外なく細胞から作られています。しかし、生物の最小ユニットである細胞は分子と呼ばれる非生物から作られています。この「非生物」から「生物」の境界線を、細胞を創ることで越えようとする研究が人工細胞研究です。細胞も人工細胞もカプセル状の脂質二重膜で形作られています(図1)。生物細胞の膜の内部にはさまざまな分子や遺伝子が詰め込まれていて、遺伝子の情報を元に生命現象を引き起こすタンパク質が作られています。これを模倣したものが人工細胞です。つまり、遺伝子の情報からタンパク質を作るために必要な全ての分子を集めて、人工的に作った脂質二重膜の中に閉じ込めることで、生きた細胞と同じ様にタンパク質を合成する擬似細胞を作ることができます。この時に重要となるのが、脂質膜を形成する技術です。人工細胞の膜を形成する脂質は主にリン脂質からできています。脂質膜を形成する方法はいろいろありますが、現在よく利用されている方法は界面通過法(またはドロップレット・トランスファー法)と呼ばれる方法です(図2)。これはリン脂質が溶けたオイルの中に細胞の内液を模した緩衝液を少量加え激しくかき混ぜることで、「ドロップレット」と呼ばれる微小な水滴がオイル中に分散した状態を作ります。リン脂質分子はリン酸基を持つ水に溶けやすい頭部と、炭化水素鎖から成るオイルに溶けやすい足部で構成されているので、オイルと水の境界面では水側に頭部が、そしてオイル側に足部が整列した1重膜を形成します。これにより脂質オイル中のドロップレットが安定に保たれます。ちょうどサラダにかけるドレッシングがこのような状態です。
このドロップレットを細胞の外液を模した緩衝液に重層すると、オイル中のリン脂質が緩衝液層との境界面でもう一つの1重膜を形成します。この状態から遠心力を利用して、ドロップレットをオイル層から緩衝液層に界面を通過させて移動します。この時、界面を通過したドロップレットの膜は1+1で2重膜になります。
ドロップレットを作る水滴の中にさまざまなタンパク質や化合物を入れることで、細胞内部の生命現象を再現することができます。例えば、無細胞タンパク質合成系の反応液(※1)を入れることで、脂質二重膜のカプセルの内部でDNAからタンパク質を合成できます。これが人工細胞です。この界面通過法を用いて現在世界中でいろいろな人工細胞が作られていますが、その細かなレシピはそれぞれの研究室で工夫されていて、論文にあまり記載されない、軽微だが重要なコツが多くありました。そのため、初めて実験をする学生や実験レシピだけを手渡された研究者が、質の高い人工細胞を再現性よくつくることは困難でした。
4. 成果
この問題に対して本研究グループは、界面通過法の実験手順を単純化することで簡単に早く人工細胞が作れる方法を編み出しました。人工細胞を上手に作るためには、リン脂質が均質に溶けた脂質オイル溶液を準備することが重要です。これまでの方法では、リン脂質が溶けているクロロホルム溶液をオイルに加え温めながら攪拌し、クロロホルムだけ蒸発させることで脂質溶液を得ていました。また他の方法では、ガラス管の中でまずクロロホルムを蒸発させ乾いた脂質フィルムを形成し、その中にオイルを加えて超音波処理をしながら温めるという方法で脂質オイルを調製していました。どちらの方法も数時間から一昼夜の時間を要していました。
今回、本研究グループが編み出した方法では、まずガラス管の中で簡易的に脂質フィルムを作り、オイルを加えたあと70度で1分間温めてすぐに撹拌するという方法に単純化しました(図3)。脂質フィルムは窒素などの不活性ガスを上から吹き付けながらボルテックス(※2)で撹拌し、できるだけ厚さの均一な脂質フィルムをガラスチューブの内壁に作ります。この状態で、吸湿と温度変化に気をつけつつ数ヶ月間保存することが可能です。オイルへの溶解は脂質の変性を避けるため、短時間で十分に解けるよう温度と撹拌時間を決定しました。この方法により、ショ糖を加えた無細胞タンパク質合成系の反応液(細胞内液)と、浸透圧を合わせた緩衝液(細胞外液)を用いて人工細胞作ったところ、今までと同等以上の人工細胞が再現性よく形成でき、内部でのタンパク質合成も観察できました(図4)。さらにDNAを除いた内液と外液を凍結乾燥することで、より早く人工細胞を形成することができました。脂質フィルムを作るところから、界面通過法で人工細胞を形成するまでわずか30分以内で完了することが可能です。これにより以前よりも格段に時短化することができました。
5. 今後の展望
本研究により、従来の方法よりも簡単かつ迅速に人工細胞を構築する手法が確立されました。また、人工細胞作製に必要な試薬を乾燥させることで、水と目的の遺伝子、卓上遠心機やボルテックスなどの簡単な機器さえあれば、どこでも人工細胞を創ることが可能になります。
合成生物学という分野で発展してきた人工細胞研究は、生命創造の可能性を秘めたエキサイティングな研究分野として大きく注目されています。光合成や二酸化炭素固定など生き物の特徴を真似た人工細胞が近年次々と報告されています。このような人工細胞研究に興味を持つ学生や、自身の研究に応用したい研究者の参入が今後ますます増えていくことが予想されます。その中で、技術的な困難さや実験設備の整備などの敷居を下げることは、この研究分野の発展を加速させるために重要です。
また、人工細胞技術のバイオエンジニアリングとしての応用は、病原性ウイルスやバクテリアの脅威が目の当たりとなった現代において、問題解決のための新しい技術として期待できます。たとえば、人工細胞キットとDNA増幅系とを組み合わせることで、サンプル中に特定の遺伝子のDNAが存在するかどうかを判別するバイオセンサーとしての応用が将来的に期待できます。今回の成果はそのためのプラットフォームとなる方法であると言えます。
【補足解説】
- ※1
- 無細胞タンパク質合成系(無細胞系):
試験管の中で転写(DNAからmRNAを合成)と翻訳(mRNAからタンパク質を合成)をするバイオツール。本研究では、転写翻訳に関わるリボソーム、30種類以上の精製酵素とアミノ酸などの低分子化合物を混合した、再構築型の無細胞系PURE system(製品名 PUREfrex🄬、ジーンフロンティア社)を使用した。
- ※2
- ボルテックス(ボルテックスミキサー):
マイクロチューブや試験管を攪拌するための実験機器。生化学の研究室で日常的に用いられる。
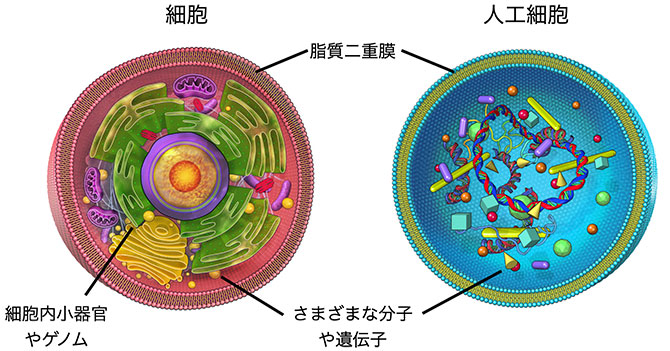
図1 細胞と人工細胞の模式図。どちらも脂質二重膜のカプセルで覆われている。細胞内にはさまざまな分子のほかに、細胞内小器官やゲノムなどが詰め込まれている。同じように人工細胞も、さまざまな分子を脂質二重膜の内部に詰め込むことで、細胞と同じような振る舞いを再現することができる。(提供:女子美術大学 佐藤暁子准教授)
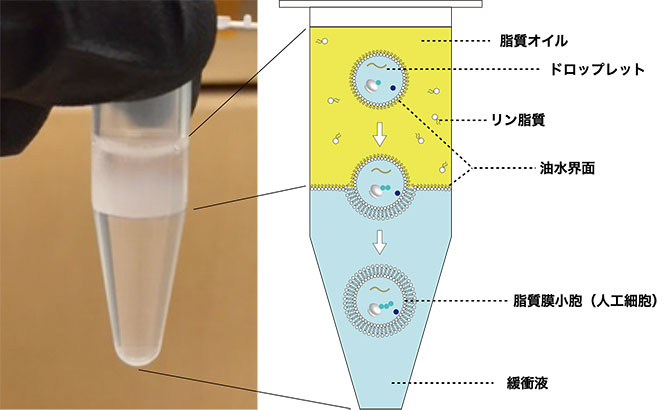
図2 界面通過法(ドロップレット・トランスファー法)による人工細胞の形成原理。左は界面通過法を行うチューブを撮影。右はその原理の説明。緩衝液上層にドロップレットを形成した脂質オイルを重層し、遠心機にかけることで人工細胞を作製する。
Sato et al., Journal of Japanese Biochemical Society 90(5): 728-733 (2018)を参考に図を作製。

図3 本手法をまとめた人工細胞作製のための実験プロトコル。
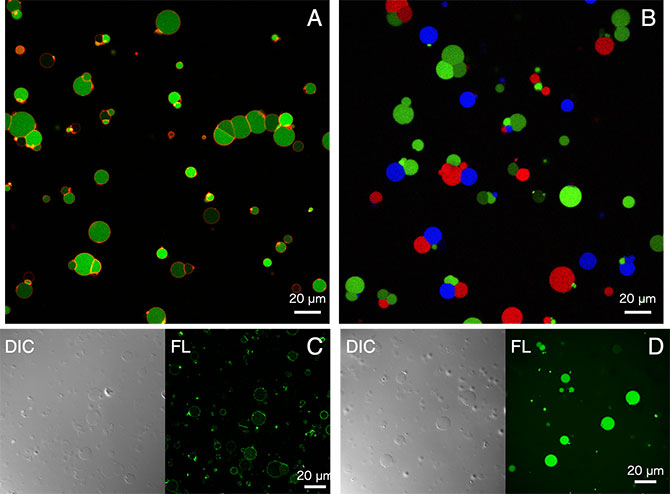
図4 本手法により作製した蛍光タンパク質を合成する人工細胞。(A)緑色蛍光タンパク質(GFP)を合成する人工細胞。赤色はローダミンでラベルしたホスファチジルエタノールアミンを含む脂質膜。(B)赤色・青色・緑色蛍光タンパク質を合成した人工細胞を混合して撮影。(C)GFPを融合した膜タンパク質を合成する人工細胞。(D)3ヶ月間常温保存した脂質フィルムを使用して作製したGFPを合成する人工細胞。人工細胞内のタンパク質合成は、PUREfrex🄬を封入し37度で3時間反応させた。Nikon社製共焦点顕微鏡システムA1Rにより撮影。DIC: 微分干渉像、FL: 蛍光画像。スケールバーは20マイクロメートル。
- 国立研究開発法人海洋研究開発機構
- (本研究について)
- 超先鋭研究開発部門 副主任研究員 車 兪澈(くるま ゆうてつ)
- (報道担当)
- 海洋科学技術戦略部 報道室